新闻中心
News Center
贝莫苏拜单抗第4个适应症获批上市,用于Ⅲ期非小细胞肺癌巩固治疗
发布时间:2026-02-14
2月14日,中国生物制药(1177.HK)核心企业正大天晴1类新药贝莫苏拜单抗注射液(安得卫®)获得国家药品监督管理局(NMPA)批准,用于在接受铂类药物为基础的同步或序贯放化疗后未出现疾病进展的未携带已知表皮生长因子受体(EGFR)敏感突变或间变性淋巴瘤激酶(ALK)重排的不可切除Ⅲ期非小细胞肺癌(NSCLC)患者的治疗。这是贝莫苏拜单抗获批上市的第4个适应症,为中国人群中放化疗免疫协同治疗的长期价值提供了新的依据。

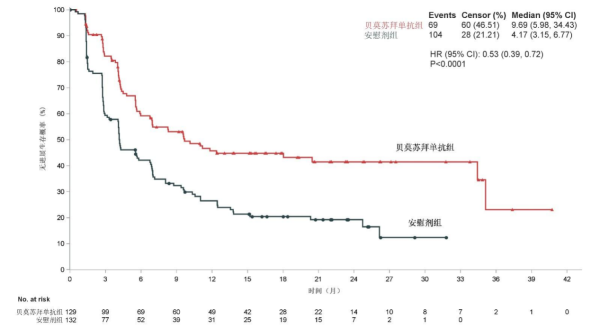
此次获批是基于R-ALPS研究取得的阳性结果。该研究纳入同步/序贯放化疗后未进展的、局部晚期/不可切除的Ⅲ期非小细胞肺癌(NSCLC)患者,其中129例患者接受贝莫苏拜单抗巩固治疗,132例患者接受安慰剂治疗直至疾病进展,主要终点是由盲态独立中心审查(BICR)评估的无进展生存期(PFS)。
研究结果[1]显示:
● 中位随访时间19.4个月,接受贝莫苏拜单抗巩固治疗的患者中位PFS为9.69个月,安慰剂组4.17个月(HR=0.53,95% CI 0.39-0.72,P<0.0001),疾病进展或死亡风险降低47%;
● 预设的亚组分析(是否吸烟、前序治疗方式为同步/序贯)显示与ITT人群获益趋势一致,展现了该治疗方案的广泛适用性;
● 总生存期(OS)数据尚未成熟,中位OS尚未达到,两组风险比HR=0.76(0.50,1.14),贝莫苏拜单抗巩固治疗组已显示出OS获益趋势;
● 安全性方面,≥3级治疗相关不良事件发生率(29.4% vs. 19.7%),为长期治疗的依从性提供了保障。
全球范围内,肺癌依旧是发病率和死亡率最高的恶性肿瘤。2022年全球肺癌发病人数248万,中国发病人数106.1万,其中NSCLC约占80%-85%,约30%的患者初诊即处于局部晚期或转移阶段[2,3]。贝莫苏拜单抗是继度伐利尤单抗、舒格利单抗之后,全球第3款已上市用于局部晚期/不可切除的NSCLC根治性放化疗后巩固治疗的PD-L1抑制剂。
目前,贝莫苏拜单抗已在国内获批4项适应症,此前已获批的适应症为联合安罗替尼(得福组合)一线治疗广泛期小细胞肺癌、复发性或转移性子宫内膜癌、一线治疗晚期不可切除或转移性肾细胞癌。此外,联合安罗替尼(得福组合)一线治疗鳞状非小细胞肺癌,以及用于晚期或不可切除腺泡状软组织肉瘤的两项适应症正处于上市审评阶段。
参考文献:
[1] Ming Chen, Yongling Ji, Long Chen, et al. R-ALPS: A randomized, double-blind, placebo-controlled, multicenter phase III clinical trial of TQB2450 with or without anlotinib as maintenance treatment in patients with locally advanced and unresectable (stage III) NSCLC without progression following concurrent or sequential chemoradiotherapy.2025 ASCO(#LBA8004).
[2] Antonia SJ, Villegas A, Daniel D, et al. Durvalumab after Chemoradiotherapy in Stage III Non-Small-Cell Lung Cancer. N Engl J Med. 2017;377(20):1919-1929.
[3] Qing Zhou,Ming Chen,et al.Sugemalimab versus placebo after concurrent or sequential chemoradiotherapy in patients with locally advanced, unresectable, stage III non-small-cell lung cancer in China (GEMSTONE-301): interim results of a randomised, double-blind, multicentre, phase 3 trial.The Lancet Oncology.2022;2(23).P209-219.
声明:
1.新闻稿旨在促进医药信息的沟通和交流,仅供医疗卫生专业人士参阅,非广告用途。
2.本公司不对任何药品和/或适应症作推荐。
3.本新闻稿中涉及的信息仅供参考,不能以任何方式取代专业的医疗指导,也不应被视为诊疗建议。若您想了解具体疾病诊疗信息,请遵从医生或其他医疗卫生专业人士的意见或指导。
前瞻性声明:
本新闻稿中包含若干前瞻性陈述,包括有关【贝莫苏拜单抗注射液(安得卫®)】的临床开发计划、临床获益与优势的预期、商业化展望、患者临床获益可能性,以及潜在商业机会等声明。“预期”、“相信”、“继续”、“可能”、“估计”、“期望”、“有望”、“打算”、“计划”、“潜在”、“预测”、“预计”、“应该”、“将”、“拟”、“会”和类似表达旨在识别前瞻性陈述,但并非所有前瞻性陈述都包含这些识别词。这些前瞻性陈述为公司基于当前所掌握的数据和信息所做的预测或期望,可能因受到政策、研发、市场及监管等不确定因素或风险的影响,而导致实际结果与前瞻性陈述有重大差异。请现有或潜在的投资者审慎考虑可能存在的风险,并不可完全依赖本新闻稿中的前瞻性陈述,该等陈述包含信息仅及于本新闻稿发布当日。除非法律要求,本公司无义务因新信息、未来事件或其他情况而对本新闻稿中任何前瞻性陈述进行更新或修改。